*仅供医学专科东说念主士阅读参考ManBetX万博体育官网在线登录
群众解读DB12更新,T-DXd为HER2+晚期脑滚动和解提供有劲把柄
乳腺癌是环球女性中发病率最高的恶性之一[1],同期亦然核心神经系统(CNS)滚动最常见的实体肿瘤之一,其中脑本色滚动尤为凸起[2]。其中,东说念主表皮滋长因子受体2(HER2)抒发是高危身分之一,与阴性(HER2-)患者比拟,HER2低抒发和HER2+患者的脑滚动风险显赫加多,发生率辨别为5.1%、8.5%及10.1%[3]。由于血脑障蔽(BBB)的存在,大部分药物难以在颅内酿成有用的药物浓度,概况有用纵容脑滚动病情进展的和解妙技有限,导致乳腺癌伴脑滚动患者的活命期相对较短。连年来,以德曲妥珠单抗(T-DXd)为代表的抗体偶联药物(ADC)药物在乳腺癌范畴快速崛起,并在HER2+和HER2低抒发乳腺癌脑滚动中获益显赫,为乳腺癌脑滚动患者带来了新的和解选择。
9月13日至17日,欧洲肿瘤内科学会(ESMO)年会在西班牙巴塞罗那广泛召开。会议本事,几项对于ADC药物和解乳腺癌脑滚动的最新究诘终结接踵公布,其中DESTINY-Breast12(DB12)究诘备受夺目。借此机会,咱们突出邀请河南省肿瘤病院闫敏莳植对乳腺癌脑滚动的策动究诘内容进行深入解读,共享独家观点。
局部和解与系统侵略:乳腺癌脑滚动的详细和解政策仍存窘境
局部和解是乳腺癌脑滚动的主要和解妙技,当今在诊疗指南中仍然是优先保举,常见的局部和解妙技包括手术、立体定向发射和解(SRS)和全脑发射和解(WBRT)等。和解有蓄意的选择主要依据多个身分,包括患者的肉体情景、CNS症状、脑滚动灶的数目、大小与散播等。局部和解的优点在于对脑滚动灶针对性强、起效马上,概况短时候内缓解患者症状;谬误在于奉陪神经理会等不良响应的风险,包括手术策动的并发症,发射和解策动损害等,且疾病进展后很难再次运用[4]。
连年来,针对HER2抒发乳腺癌脑滚动的一些系总揽疗有蓄意,包括化疗、大分子单克隆抗体、小分子酪氨酸激酶扼制剂(TKI)和ADC均在HER2+乳腺癌脑滚动患者中进行了探索。其中因受限于BBB的通透性,大分子抗HER2单克隆抗体高剂量曲妥珠单抗和帕妥珠单抗聚合用于乳腺癌脑滚动的客不雅缓解率(ORR)仅为11%[5]。小分子TKI药物聚合有蓄意获取了相对较高的ORR,不同经由地蔓延了患者的中位无进展活命期(mPFS),约为3.1-11.3个月[6-9],其中以PERMEATE究诘探索的吡咯替尼聚合卡培他滨有蓄意和解新发脑滚动获取了不弱于局部和解的近期和始终疗效,在未经放疗的乳腺癌脑滚动患者中,颅内ORR(iORR)可达到74.6%[7],中位总活命期(mOS)为35.9个月[10],展现了系总揽疗在乳腺癌脑滚动中的疗效,指示了乳腺癌脑滚动系总揽疗的新标的。此外,新式靶向HER2的ADC药物T-DXd在HER2+和HER2-low的脑滚动和解中也进行了初步探索。
既往究诘说明:ADC药物为HER2+乳腺癌脑滚动患者提供新的和解想路
T-DXd是由曲妥珠单抗和高活性拓扑异构酶I扼制剂载药通过可裂解的四肽运动子偶联而成的新式ADC药物。前期临床前究诘标明[11],T-DXd在HER2+乳腺癌脑滚动PDX小鼠模子中深入馅CNS和解活性。既往多项临床究诘标明,T-DXd在HER2+乳腺癌脑滚动患者中体现出邃密疗效,在和解乳腺癌脑滚动方面积蓄了丰富的循证把柄。
2023年ESMO大会上公布了一项汇总DB01、02和03究诘中基线伴脑滚动患者的疗效的探索性汇总分析[12],包括既往接管和解的踏实性脑滚动患者和未接管和解的举止性脑滚动患者。究诘终结深入在踏实性脑滚动患者中,T-DXd组的iORR为45.2%,中位CNS PFS为12.3个月,比拟对照组镌汰了41%的CNS进展或厌世风险;在举止性脑滚动患者中,T-DXd组的iORR为45.5%,中位CNS PFS为18.5个月,比拟对照组镌汰CNS进展或厌世风险81%。
一些真确寰宇究诘和小样本前瞻性究诘探索了T-DXd在HER2+乳腺癌脑滚动中的疗效。此外,一项纳入10项T-DXd和解HER2+乳腺癌脑滚动患者究诘的集会分析 [13]中,患者包括128例举止性脑滚动,169例踏实性脑滚动。终结深入T-DXd用于HER2+乳腺癌脑滚动的mPFS为15个月,在踏实性和举止性脑滚动患者亚组中,ORR辨别为64%和61%(P=0.78),这项究诘终结为T-DXd在HER2+乳腺癌脑滚动患者的运用提供了真确寰宇的把柄。
一项前瞻性II期临床西席的TUXEDO-1究诘中,纳入了15例HER2+乳腺癌举止性脑滚动患者, 总体CNS ORR为73.3%[14],中位随访26.5个月后,患者mPFS为21个月[15],指示T-DXd在举止性脑滚动患者中的邃密疗效。
2024年ESMO公布的DB12究诘,初次展示了T-DXd和解乳腺癌脑滚动患者的大型前瞻性究诘终结。
DB12数据再证:T-DXd在脑滚动乳腺癌患者中的耐久疗效

DB12是一项IIIb/IV期究诘,评估了T-DXd 在既往接管过和解的HER2+晚期乳腺癌患者中的疗效和安全性 [16]。究诘共纳入504名受试者,根据是否存在脑滚动将其分为两组:脑滚动队伍(263例)和非脑滚动队伍(241例)。基线脑滚动队伍的主要额外是PFS,次要额外包括CNS PFS、CNS ORR和ORR(基线伴脑滚动队伍)以及安全性。
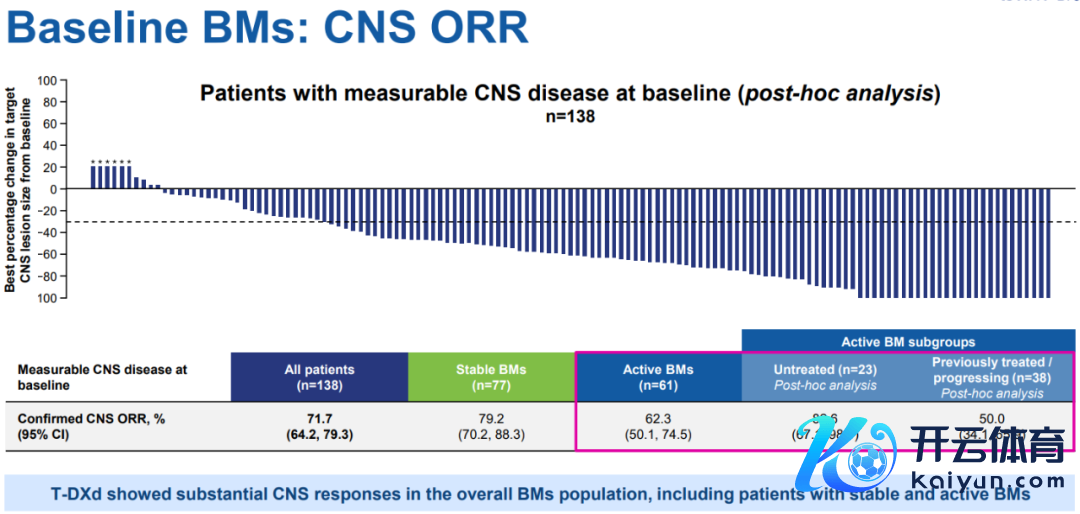
终结深入,脑滚动队伍mPFS达到了17.3个月,12个月PFS率为61.6%,12个月CNS PFS率与之相配,达到58.9%,意味着T-DXd全身和颅内疗效极端接近;在脑滚动患者中,77例踏实性脑滚动的CNS ORR为79.2%;61例举止性脑滚动患者的CNS ORR为62.3%,其中未经和解的举止性脑滚动23例,CNS ORR高达82.6%。
尽管该究诘为非当场对照究诘,但该究诘终结和纳入患者群体却有进击参考价值,不仅为临床和解乳腺癌脑滚动提供了新选择,也增强了对系总揽疗有蓄意的信心,或将为乳腺癌脑滚动带来新的和解旅途,并对临床和解带来新的想索。
寻踪觅迹:ADC药物在脑滚动肿瘤中的机制辩论
由于BBB的存在,大分子药物每每在颅内抗肿瘤活性方面阐发欠安,难以在脑本色内酿成有用的药物浓度。2024年AACR大会公布的一项临床前究诘奋发于辩论ADC大分子药物是否有才调有用穿越BBB并阐发抗肿瘤活性[17],究诘终结展示了TROP2 ADC药物Dato-DXd对小鼠模子颅内肿瘤的扼制终结显着,况且不错散播到局部肿瘤微环境中。新式ADC在乳腺癌脑滚动中的疗效,可能收成于本人的特质极端私有结构。通过可裂解运动子以及膜通透性载荷,使其概况参预CNS,以及肿瘤旁不雅者杀伤效应达到平时的杀伤终结。也可能受到其他身分(如DAR)的影响,领有高药物偶联比(DAR)的ADC药物,比拟于低DAR的ADC药物,能显赫普及在CNS中的寄递效力及抗肿瘤终结[18]。不同ADC药物在脑滚动中的疗效不尽疏导,究诘标明核心神经系统对ADC药物的接纳具有很大的异质性[19,20]。载荷同为拓扑异构酶扼制剂的SHR-A1811在一项前瞻性、多队伍究诘中,单药队伍25例HER2+乳腺癌脑滚动患者的CNS ORR达到84%[21],为以拓扑异构酶扼制剂为载荷的ADC药物在脑滚动中的有用性提供了互相印证的数据。
聚合和解新前沿:ADC药物在HER2+乳腺癌脑滚动中的新机遇
当今,以T-DXd为代表的新式ADC药物积蓄了丰富把柄,在HER2+脑滚动患者中不雅察到了较高的ORR,概况马上减小颅内肿瘤体积,为患者提供了减速局部和解(尤其是全脑放疗)的机会,同期也为临床和解旅途带来新的想考,若何衡量局部和解与全身和解带给患者的获益,更准确田主理局部和解和系总揽疗的切入时机,制定出最合乎患者的和解策动。
ADC药物在单药和解获取显赫进展的同期,也在聚合和解政策上伸开了积极探索,对脑滚动患者提供了新的潜在和解标的。当今,多个策动究诘正在进行中,举例单臂、洞开标签的II期究诘HER2CLIMB-04旨在评估T-DXd聚合图卡替尼的协同作用[22];单臂SHR-A1811前瞻性、多队伍究诘中,也在探索SHR-A1811聚合吡咯替尼、SHR-A1811聚合贝伐珠单抗对HER2+乳腺癌脑滚动的疗效(NCT05769010)。这些究诘正在积极鞭策,期待明天有更多临床数据发布。这些聚合和解政策有望提高疗效、克服单一疗法所面对的耐药性问题,进一步推动HER2+乳腺癌脑滚动药物和解政策,为患者带来新的但愿,也为临床医学提供更为高大的和解视角。
群众简介

闫 敏 莳植
河南省肿瘤病院乳腺科,河南省乳腺病诊疗中心 副主任
主任医生 医学博士
中国临床肿瘤学会(CSCO)乳腺癌群众委员会 常务委员
中国女医生协会乳腺疾病究诘中心专科委员会 常务委员
中国医生协会肿瘤医生分会乳腺癌学组 常务委员
中国医药莳植协会肿瘤滚动专科委员会 常务委员
中国抗癌协会多原发和不解原发肿瘤群众委员会 委员
国度卫生健康委才调建设和陆续莳植肿瘤学群众委员会 委员
中国究诘型病院学会精确医学与肿瘤MDT专科委员会乳腺学组 副主任委员
河南省肿瘤诊疗质料纵容中心乳腺癌群众委员会 副主任委员
河南人命柔软协会乳腺专科委员会 副主任委员
河南省病院协会乳腺疾病惩办与改进分会 副主任委员
精彩资讯等你来
参考文件:
[1] Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024 Apr 4.
[2] Wanleenuwat P, Iwanowski P. Metastases to the central nervous system: Molecular basis and clinical considerations. J Neurol Sci. 2020 May 15;412:116755.
[3] Guven DC,Kaya MB,Fedai B,et al.HER2-low breast cancer could be associated with an increased risk of brain metastasis.Int J Clin Oncol.2022 Feb;27(2):332-339.
[4] Garcia-Alvarez A, Papakonstantinou A, Oliveira M. Brain Metastases in HER2-Positive Breast Cancer: Current and Novel Treatment Strategies. Cancers (Basel). 2021 Jun 11;13(12):2927.
[5] Lin NU, Pegram M, Sahebjam S, Ibrahim N, Fung A, Cheng A, et al. Pertuzumab Plus High-Dose Trastuzumab in Patients With Progressive Brain Metastases and HER2-Positive Metastatic Breast Cancer: Primary Analysis of a Phase II Study. J Clin Oncol. 2021;39(24):2667–75.
[6] Bachelot T, Romieu G, Campone M, Diéras V, Cropet C, Dalenc F, et al. Lapatinib plus capecitabine in patients with previously untreated brain metastases from HER2-positive metastatic breast cancer (LANDSCAPE): A single-group phase 2 study. Lancet Oncol. 2013;14(1):64–71.
[7] Yan M, Ouyang Q, Sun T, Niu L, Yang J, Li L, et al. Pyrotinib plus capecitabine for patients with human epidermal growth factor receptor 2-positive breast cancer and brain metastases (PERMEATE): a multicentre, single-arm, two-cohort, phase 2 trial. Lancet Oncol [Internet]. 2022 Mar;23(3):353–61.
[8] Freedman RA, Gelman RS, Anders CK, Melisko ME, Parsons HA, Cropp AM, et al. TBCRC 022: A phase II trial of neratinib and capecitabine for patients with human epidermal growth factor receptor 2-positive breast cancer and brain metastases. J Clin Oncol. 2019;37(13):1081–9.
[9] Lin NU, Borges V, Anders C, Murthy RK, Paplomata E, Hamilton E, et al. Intracranial efficacy and survival with tucatinib plus trastuzumab and capecitabine for previously treated HER2-positive breast cancer with brain metastases in the HER2CLIMB trial. J Clin Oncol. 2020;38(23):2610–9.
[10] Min Yan, Quchang Ouyang, Tao Sun, et al. Pyrotinib plus capecitabine for patients with HER2-positive metastatic breast cancer and brain metastases (PERMEATE trial): overall survival results from a multicenter, single-arm, two-cohort, phase 2 trial,eClinicalMedicine, Volume 76, 2024, 102837.
[11] Kabraji S, Ni J, Sammons S, et al. Preclinical and Clinical Efficacy of Trastuzumab Deruxtecan in Breast Cancer Brain Metastases. Clin Cancer Res. 2023 Jan 4;29(1):174-182.
[12] Hurvitz S.A,Modi S,Li W,et al.A pooled analysis of trastuzumab deruxtecan(T-DXd)in patients(pts)with HER2-positive(HER2+)metastatic breast cancer(mBC)with brain metastases(BMs) from DESTINYBreast(DB)-01,-02,and-03.2023 ESMO 377O.
[13] Michelon I.F,Vilbert M.S,Marinho A.D,et al.Trastuzumab deruxtecan for HER2-positive breast cancer brain metastasis:A systematic review and meta-analysis.2023 ESMO 414P.
[14] Bartsch R, Berghoff AS, Furtner J, et al. FINAL OUTCOME ANALYSIS FROM THE PHASE II TUXEDO-1 TRIAL OF TRASTUZUMAB-DERUXTECAN IN HER2-POSITIVE BREAST CANCER PATIENTS WITH ACTIVE BRAIN METASTASES. 2023 SABCS PO2-04-05.
[15] Bartsch R, Berghoff AS, Furtner J, et al. Final outcome analysis from the phase II TUXEDO-1 trial of trastuzumab-deruxtecan in HER2-positive breast cancer patients with active brain metastases. Neuro Oncol. 2024 Jul 4:noae123
[16] Lin N, Ciruelos E, Jerusalem G, et al. Trastuzumab deruxtecan (T-DXd) in patients (pts) with HER2+ advanced/metastatic breast cancer (mBC) with or without brain metastases (BM): DESTINYBreast-12 primary results. 2024 ESMO LBA18.
[17] K. Jones, M. Suksomboon, S. rosenthal, et al. Dato-DXd mediates anti-tumor activity in preclinical TROP2-expressing intracranial tumor model. 2024 AACR Abstract 1911.
[18] Anami Y, Otani Y, Xiong W, et al. Homogeneity of antibody-drug conjugates critically impacts the therapeutic efficacy in brain tumors. Cell Rep. 2022;39(8):110839.
[19] Marin, B.-M. et al. Heterogeneous delivery across the blood-brain barrier limits the eficacy of an EGFR-targeting antibody drug conjugate in glioblastoma. Neuro Oncol. 23, 2042–2053 (2021).
[20] Gril, B. et al. HER2 antibody-drug conjugate controls growth of breast cancer brain metastases in hematogenous xenograft models, with heterogeneous blood–tumor barrier penetration unlinked to a passive marker. Neuro Oncol. 22, 1625–1636 (2020)
[21] Min Yan, Huimin Lv, Limin Niu, et al. Efficacy and safety of HER2-ADC SHR-A1811 in HER2-positive breast cancer with brain metastases.Journal of Clinical Oncology, Volume 42, 16_suppl.e13006
[22] Krop IE,Ramos j,Zhang CY,et al.HER2CLIMB-04: Phase 2 open label trial of tucatinib plus trastuzumab deruxtecan in patients with HER2+ unresectable locally advanced or metastatic breast cancer with and without brain metastases. 2021 ASCO. TPS1097.
* 此文仅用于向医学东说念主士提供科学信息,不代表本平台不雅点
